每日经济新闻 2021-07-12 09:37:13
每经记者|金喆 实习生 黄颖琳 每经编辑|文多

■相关公司:科济药业-B(02171,HK)
■市值:185.81亿港元(截至7月9日收盘)
■核心竞争力:
出色的差异化CAR-T细胞疗法管线;
升级的全人抗BCMA CAR-T疗法具有良好的疗效和安全性;
针对实体瘤的潜在全球同类首创CLDN18.2 CAR-T候选产品;
治疗HCC的潜在全球同类首创GPC3 CAR-T候选产品
■机构眼中的公司:
CAR-T细胞疗法领域的领导者;领先的创新CAR-T细胞治疗企业(安信国际)
■所属板块:生物制药
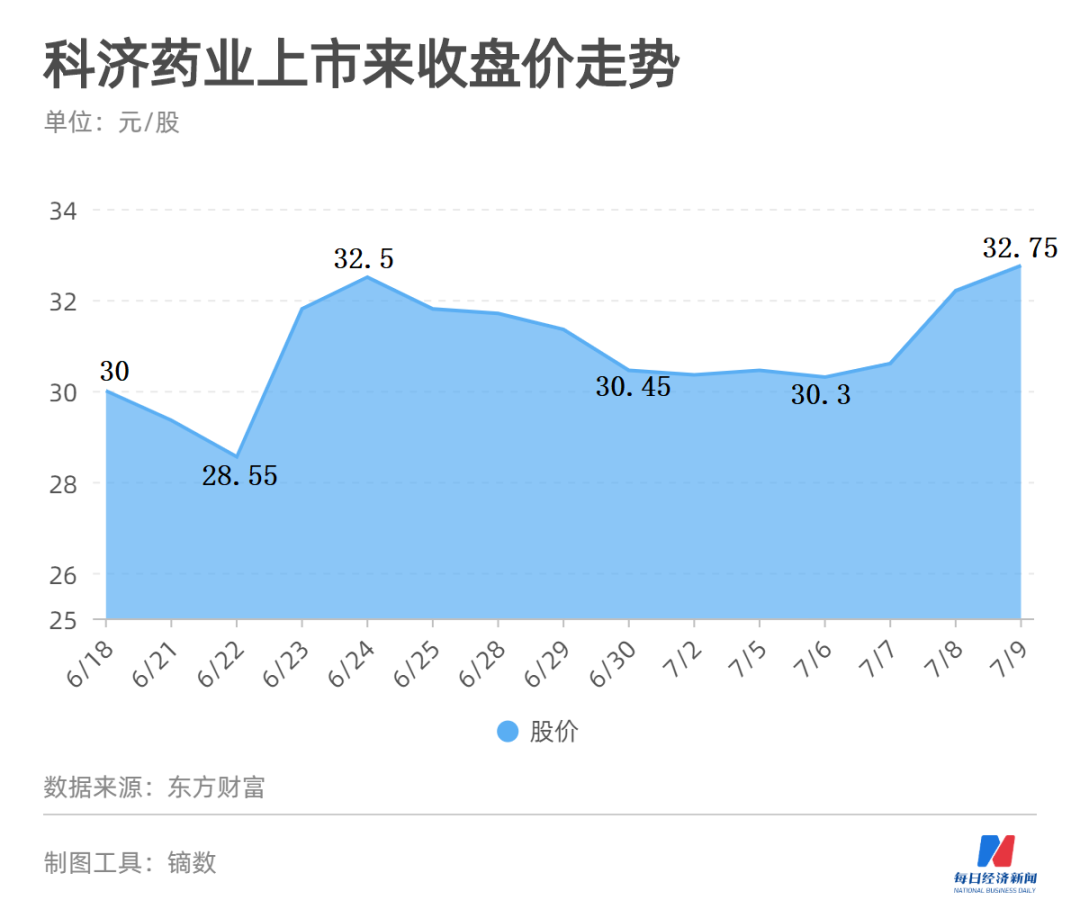
6月18日,科济药业-B(02171,HK)在港交所挂牌上市,成为又一家暂未盈利的生物制药上市企业。在生物制药领域,这家成立不到8年的公司早已名声大噪——它在中国所有CAR-T公司中获得IND临床试验批件数排名第一。但在资本市场,科济药业上市后没能受到追捧,上市首日盘中跌幅一度逾18%,与上市前夕超400倍初步认购的火爆场面大相径庭。截至7月9日,科济药业的股价较发行价还略低0.05元。
是创新药赛道不香了吗?还是市场对CAR-T细胞疗法的前景有所观望?亦或是科济药业的创新成色不被认可?带着投资者的这些疑问,《每经人物·专访董事长》栏目记者专访了科济药业董事长李宗海,由他来对上述疑问进行解答。

为何 选择CAR-T疗法:
希望做出治愈肿瘤病人的药

如果没有在港交所挂牌上市,大多数人可能都没听说过科济药业。
而对于刚上市就遇上破发,李宗海也知道,是二级市场对CAR-T这个赛道还需要时间理解。
李宗海自己提起了一连串的设问:“比如,实体瘤CAR-T是否能成功?CAR-T在不同国家和地区的商业化挑战和痛点是什么?科济的创新技术是否能解决这些挑战,在国际上处于一个什么位置?如何来前瞻性地判断一个未盈利CAR-T公司的发展前景?在美国,有的没有任何项目进入临床试验阶段的公司,上市时市值可达到数十亿美元,其原因是什么?那么,科济的原创性技术平台的价值如何?”
在这么多的问题面前,他认为,一方面需要二级市场花更多时间去理解这个行业,另一方面科济药业也会和二级市场加强沟通交流。
要解答这些问题,或许可以先从公司的诞生说起。科济药业是中国第一批迈入细胞治疗产业的企业之一,由在海外留学和工作20多年的李宗海创办于2014年10月。创办这家公司,也是李宗海读书时候的梦想。
上世纪90年代,李宗海从医学院即将毕业时就在思考自己能做些什么有价值的事情。“当时身边有不少肿瘤患者,我自己也有些体会,但那会的肿瘤治疗远没有像今天这样火热,一些医院甚至连肿瘤科、保健药都没有,我当时的信念就是能不能做一点改变。”李宗海回忆说。
过去10年,中国创新药研发从萌芽到爆发通常分成四类,从Me too(仿制)到Me-better(仿制中创新)、再发展为Best-in-class(同类最佳),最后到First-in-class(创新)。很多创始人都面临这样的选择题,到底是先研发出成药难度低、能够尽快上市的Me too,还是挑战无人之地的First-in-class。
李宗海却没有陷入过这种纠结中,他脑海中创新的标准只有一条,就是“能不能治愈病人”。
“这很重要,你要创新,如果说别人已经在做了你再做,不是说它没有价值,坦率来说我认为价值不是那么大。”李宗海表示,2010年以前的晚期肿瘤治疗方式包括化放疗以及直接靶向肿瘤的单克隆抗体/小分子药物等,能够延长患者的生存期,但大多不能治愈,他的初衷是希望能开发更有效的、能够治愈的抗肿瘤药物。
至于公司为什么选择了CAR-T细胞疗法,就与他的这一初衷有关。
CAR-T细胞疗法是指通过基因改造技术,在人体T免疫细胞上加入一个嵌合抗原受体(CAR),CAR-T细胞在实验室扩增后再重新注入到患者体内,不仅能识别癌症细胞,同时也可触发免疫系统将癌细胞杀死(如下图)。
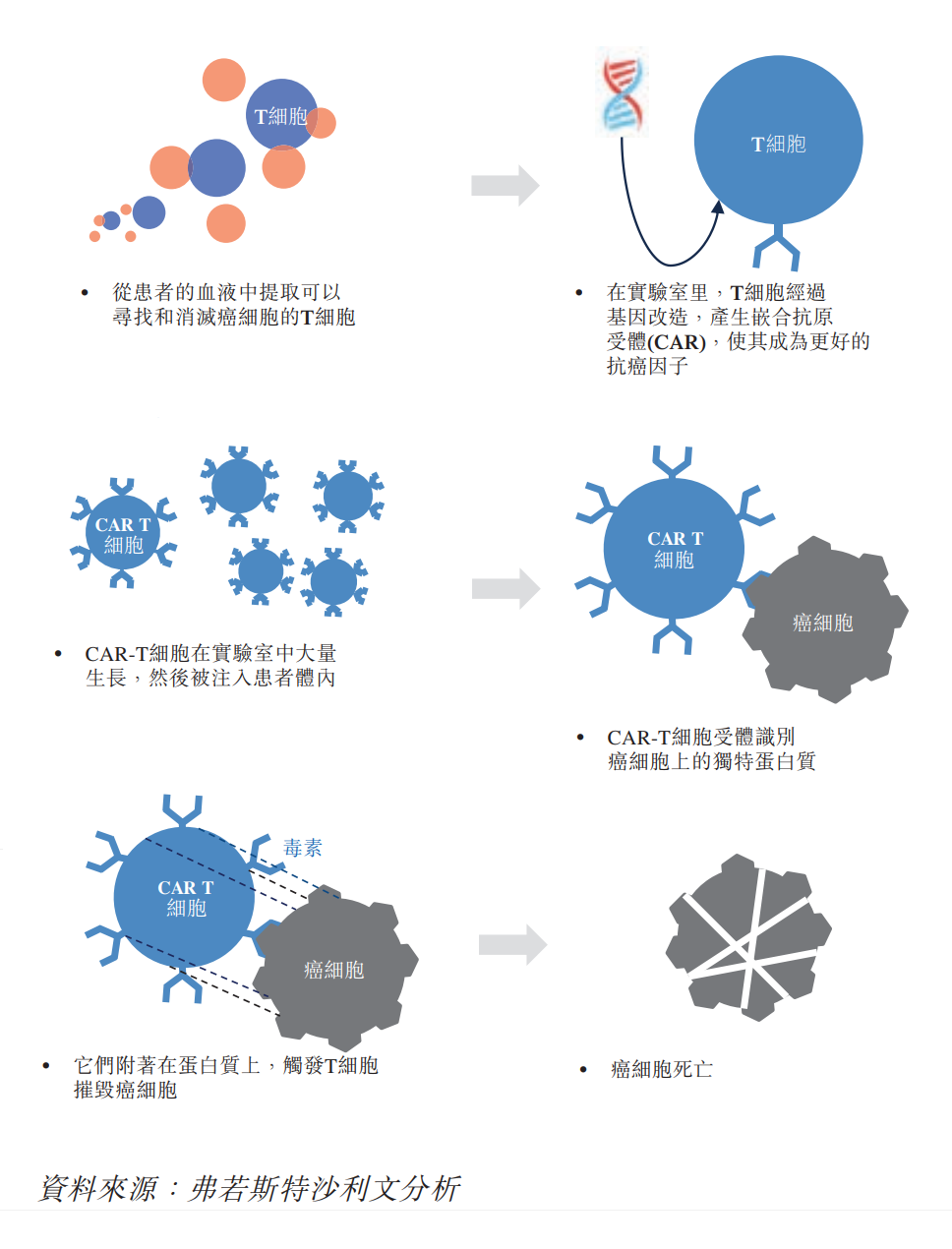
图片来源:科济药业招股书截图(有微调)
过去20多年,李宗海尝试过基因治疗、单抗、双抗和抗体药物偶联物,最终选定了CAR-T细胞疗法的研发方向。在这个过程中,他发现CAR-T抗肿瘤活性非常强大,最后可能开发出治愈肿瘤患者的药物。于是在10多年前,他和团队最终决定专注于CAR-T药物的研发。
如今,李宗海被业内称为“CAR-T细胞免疫治疗开拓者”之一。他在国际上率先开发了靶向GPC3、靶向CLDN18.2的CAR-T细胞等,适应症覆盖肝癌、胃癌、胰腺癌、肺鳞癌等恶性肿瘤,发表百余篇论文,是两百多件发明专利的发明人。而科济药业,已在中国、美国和加拿大获得7项CAR-T疗法的IND许可,在中国所有CAR-T公司中排名第一。
在李宗海看来,这是真正有望治愈癌症的药物。但是,目前世界上对CAR-T的成功应用多集中在血液肿瘤上,而占所有肿瘤90%以上的实体瘤领域却有难题迟迟难以攻克。血液瘤的病人,比如何杰金氏淋巴瘤病人,80%以上可以治愈,而实体瘤,比如胃癌病人,则整体预后较差。晚期胃癌患者5年生存率仅5%~20%,用传统化疗实现治愈是基本不可能,他希望攻克的目标,便是让CAR-T免疫细胞疗法可以给胃癌患者带去希望。
他经常把血液瘤比喻成散兵游勇,更容易各个击破,把实体瘤比喻成“黑社会团体”,由于其更加复杂的肿瘤微环境,对CAR-T造成了更大的挑战。但李宗海坦言,尽管有这样的挑战,但既然有医疗需求,就需要有人去做这个事。
他的想法就是付一生之努力去尝试,“不知道会不会成功,但我们知道会做一些贡献,也许我们往前迈进5步,(以后)再有人再迈进5步,就达到了” 。

突围CAR-T赛道:
挑战实体瘤,有望率先破冰

2014年科济药业选择CAR-T赛道时,国内还没有多少人关注到细胞治疗领域,如今,它已经是细胞治疗行业的重要分支。
兴业证券在研报中指出,截至2021年4月16日,全球共有2073种活性细胞治疗药物研发管线,比2020年同期增加572种。目前,美国和中国对于细胞治疗的研究数量为全球最多,2021年美国学术研究、商业研究数量分别为137起、654起,而中国为275起、420起。
《每日经济新闻》记者了解到,截至2021年6月25日,美国FDA已批准5款CAR-T治疗产品上市,其中4个靶向CD19靶点,1个靶向BCMA,均用于治疗血液瘤。从价格角度来看,目前5款CAR-T治疗产品的定价同样高昂,降低了可触及的人群。
除了上市产品,血液瘤赛道的拥挤还体现在临床阶段——在全球开展的CAR-T临床中,72%针对血液瘤,针对实体瘤的仅占比28%。而在中国,这种扎堆研发的情况更加明显,数据显示,围绕CD19和BCMA两个靶点,已经进入临床试验的相关记录就分别有138条、38条,超过80%的产品以CD19为靶点。只有两个实体瘤CAR-T获得IND批件,而它们均来自于科济药业。
《每日经济新闻》记者了解到,这与CAR-T在实体肿瘤治疗中面临的多种瓶颈有关。其中最大的难点,就是如何让CART细胞突破实体瘤的微环境,在病灶内大规模增殖并消灭癌细胞。这也正是很多企业对实体瘤应用的研发望而却步的原因。
李宗海希望挑战这样的医学盲区。他指出,实体瘤的治疗难度比血液瘤更大,例如合理靶点的选择、肿瘤微环境的克服等,均导致实体瘤研发进展缓慢。但实际上约90%癌症发病率是由实体瘤引起。
科济药业在全球第一个成功识别、验证和报告CLDN18.2和GPC3作为CAR-T疗法的合理肿瘤相关抗原,这些抗原分别用于胃癌/胰腺癌和肝细胞癌。其自主研发的CT041就是针对实体瘤、潜在全球同类首创、靶向CLDN18.2 CAR-T的候选产品。
招股说明书显示,CT041在2020年获得美国FDA授予的孤儿药产品资格认定,用于治疗胃癌/食管胃结合部腺癌。2021年获得EMA授予的孤儿药产品资格认定,用于治疗胃癌。临床数据更新显示,22名胃癌/食管胃结合部腺癌患者(18名三线及以上治疗、4名二线治疗)中,客观缓解率(ORR)为50%,无药物相关死亡。

图片来源:科济药业招股书截图(有微调)
在科济药业现有自主研发管线中,有7个CAR-T候选产品用于治疗实体瘤,其中2个均做到了全球潜在First-in-class(同类首创),分别是上面提到的CT041,以及针对肝细胞癌(HCC)的CT011。如果这2款产品能顺利上市,科济药业将填补CAR-T细胞疗法在实体瘤治疗方面的空白。
李宗海回忆这一路的研发历程后感慨道,当时也遇到了很多挑战,也会面临研究的盲区,虽说细胞治疗领域还是比较开放的,拥有更多的机会去调整和尝试,但也需要更长的开发周期。
2015年,科济药业开始做肝癌、胶母细胞瘤等方面的临床试验,第二年1月就拿到了3000万美元的融资。李宗海觉得他们十分幸运,毕竟,那时候市场对细胞治疗的理解程度不比现在,很少人觉得会成功。
在对科济药业持续大半年的尽调过程中,正心谷资本最终在更大样本的情况下,验证了科济核心产品的突破性的疗效与安全性优势,验证了他们对于公司核心产品的Best-in-class/First-in-class判断。至于选择科济药业,直接关键因素在于公司整体出色的研发管线,包括无论疗效还是安全性都具备有优势的BCMA CAR-T,以及已经具有突破性疗效数据的CLDN18.2 CAR-T。

图片来源:视频截图
“资本的介入是我们发展的动力,确实会有一些压力,但整体还是推进比较顺利,他们也很理解我们。”李宗海如此表示。

新药上市时间表:
预计明年上半年递交首个申请

“今天是好日子”,2020年12月8日,李宗海在朋友圈写下一段话,这一天,上海全部降为低风险地区。同时,科济药业的在研药物CT053全人抗BCMA自体CAR-T细胞注射液通过了国家药品监督管理局药品审评中心公示期,正式纳入突破性疗法药物品种,拟定适应症为复发难治性多发性骨髓瘤。
CT053是科济药业研发进度最快的药物,招股书显示,由于尚未产品商业化销售,且并无产生任何收益,科济生物处于亏损状态。截至2019年及2020年底,经营亏损分别为2.27亿元和3.27亿元,几乎全部亏损由研发开支及行政开支所致。而预计CT053在2022年和2023年,会分别在中国、美国递交NDA和BLA申请。
但一个不容忽视的情况是,国内CAR-T领域的竞争也日渐激烈,目前已有28家企业开展CAR-T细胞治疗产品的临床试验,而且存在同质化靶点扎堆的情况。在2021年6月23日,复星凯特引进的Yescarta获得国家药监局批准,成为中国首款CAR-T细胞治疗产品,用于治疗二线或以上系统性治疗后复发或难治性大B细胞淋巴瘤成人患者。
与此同时,CAR-T细胞疗法的市场容量短期内不会超过50亿元。兴业证券报告指出,中国CAR-T市场有望在2021年启动增长,市场规模为2亿元,未来,在政策优惠和患者负担能力提高的推动下,2024年和2030年市场规模将分别进一步增长至53亿元和289亿元。
这意味着,国内CAR-T研发赛道的竞争程度不亚于PD-1。在李宗海看来,这种同质化现象不止在中国存在,全球亦是如此。因为人体天然的靶点只有这么多,合适的靶点非常有限,使得企业涌入相同赛道。最终判断一个药品能否上市,还是以安全性和疗效作为标准。
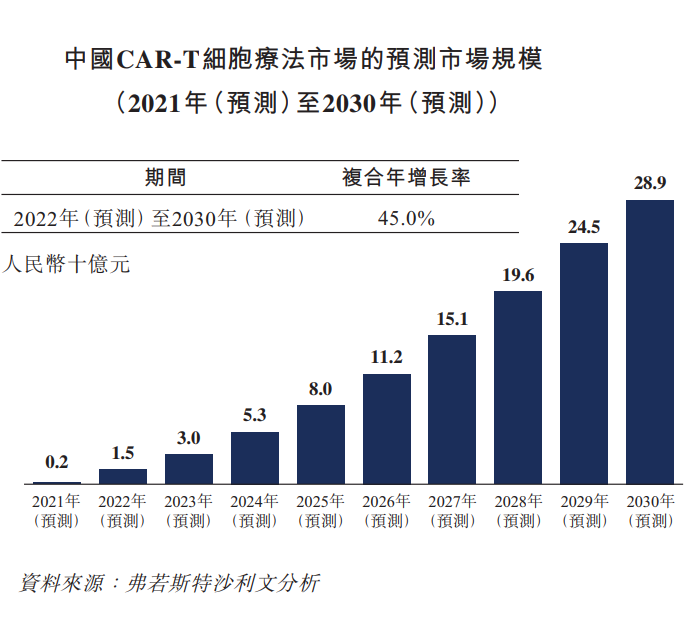
图片来源:科济药业招股书截图(有微调)
对于所有生物科技从业者来说,把产品从研发推向上市还只是第一步,更能体现产品价值的是上市后的商业化。李宗海向记者透露,目前市场部门已有人到岗,预计在2022年底进一步将销售及营销团队扩充至70人以上。在他看来,团队成员的数量是充足的,因为CAR-T覆盖医院的数量较少,主要是国内一些顶级的大医院。此外,李宗海也把目光放到全球化的布局上,计划建立美国等国外主要市场的销售和营销力量。
“医生认可通往商业化道路的重要性,目前与科济生物BCMA CAR-T临床合作的医院大概有20家,对于临床来说,他们也在等待上市。”李宗海提到,以BCMA CAR-T为例,这种细胞治疗方法已经写进治疗指南中,很多医生也已接触到BCMA CAR-T,并且看到其疗效是颠覆性的、前所未有的,可以给病人提供真正的帮助,甚至有可能治愈。这对于医生来讲是很大的动力,因此他们的接受度是很高的。

漫谈创新:
它给了公司尝试国际化的勇气

过去6年,从一年抗体药申报不超过两位数,到如今PD-1、ADC甚至双抗和CAR-T等前沿每个新药都有数十家企业布局,中国创新药迎来黄金发展时期。
李宗海对《每日经济新闻》记者表示,2015年,药政改革开启行业新纪元后,国内创新药开始进入发展快车道。起初,创新药研发以热门靶点为主,同质化严重,竞争赛道非常拥挤。对这一局面,李宗海觉得不难理解,因为创新能力是需要时间培养的,“你让一个团队突然做一个核心,谈何容易。相较之下,国外积累时间更长,因此他们的技术储备会更强”。
在发展过程中,国内的资源配置也在不断优化。他认为,以前更多的资源是放在Me too或者Me better上,但在医保谈判的背景下,传统价格体系受到冲击。后来生物类似药市场开始火热,其在商业化渠道上更强,导致仿制药基本上很难有太大的竞争力,资源才开始倾斜到创新研发上。
此外,终端支付能力也是影响创新推动的重要因素之一。在李宗海看来,中国的终端支付能力还不足,中国创新药市场占有率和市场规模面临瓶颈,利润率最终也会比较低。“如果一个药厂没有终端的回报,怎么可能有持续的创新呢?如果按照国内的价格,获得可观经济回报的挑战还是比较大的。”
2020年开始,国内创新药企开始谈起国际化,把商业化方向放到了高药品定价的欧美国家。在李宗海看来,现在的核心技术主要还是来自西方国家,中国药企需要拒绝拿来主义,在技术上有自己的创新。中国创新药需要不断地成长,但也不能妄自菲薄。近年来,国内有越来越多的创新药产品和公司走向全球,这种“出海”的底气便来源于创新能力的提高。“因为有创新,我们才有勇气去尝试国际化。”李宗海谈到,2016年科济生物在美国Delaware注册子公司,成为中国CAR-T领域首家到美国建立子公司的药企。

图片来源:视频截图
摆在李宗海面前的一个现实问题是,因为价格过高,很多患者并不一定能用上CAR-T药物。《每日经济新闻》记者了解到,诺华用于治疗白血病的Kymriah定价为治疗一次47.5万美元;吉利德/Kite用于治疗B细胞淋巴瘤的Yescarta治疗费用定价为治疗一次37.3万美元。这些CAR-T药物在美国均已经进入医保。而复星凯特近期获批的Yescarta,也被传定价高达人民币120万元。
李宗海希望科济药业能够增强CAR-T药物的可及性,这对于很多做药者来说,在某种意义上是良心的拷问。面对高昂的治疗成本,科济药业的对策是:以药物的良好安全性降低非产品相关治疗药物成本;多管线产品及大适应症带来规模效应;以及通过端对端生产能力,包括自主生产慢病毒载体等来降低CAR-T的制造成本;长远来看,希望通过同种异体通用CAR-T技术THANK-uCAR(THANK-uCAR指公司专有技术生产的CAR-T细胞较源自第三方捐献者的T细胞具有更好的扩增性及持久性)来降低成本。与此同时,随着中国经济实力的提升,以及商业保险等方式的介入,将有望进一步提升CAR-T药物可及性。
在李宗海看来,细胞治疗会成为未来癌症治疗的主流手段。他把细胞治疗比喻为一个大卡车,可以在里面装载很多东西。比如说靶向性问题,用传统技术基本上是不可能攻克的,但细胞治疗可以把你想象到的现代生物分析技术整合在一起,可以通过合成生物学、基因编辑等技术去调控靶向。另外,它的灵活性较强,对其他疾病如自身免疫疾病、心血管疾病等,都有可能涉及和攻克。

记者手记丨罗马非一日建成 药品创新任重道远
就像科济药业董事长李宗海所说,创新能力需要时间培养,虽然国内越来越多的创新药产品和公司走向全球,但现在的核心技术多数还不在我们手上。
中国药企渴望在技术上有自己的创新,也需要有自己的创新,只有掌握更多核心技术,避免拿来主义,才可能在全球创新药的舞台越走越远。
我们期待更多像科济药业这样的创新药企业诞生,渴望有更多的First-in-class研发上市,也渴望有更多新药、好药上市,提升药物可及性。但这一切,都需要我们扎实做好基础研究,给创新多一些耐心,给创新多一些时间。
记者:金喆 实习生 黄颖琳
编辑:文多
视觉:刘阳
视频编辑:祝裕
排版:文多 马原
如需转载请与《每日经济新闻》报社联系。
未经《每日经济新闻》报社授权,严禁转载或镜像,违者必究。
读者热线:4008890008
特别提醒:如果我们使用了您的图片,请作者与本站联系索取稿酬。如您不希望作品出现在本站,可联系我们要求撤下您的作品。
欢迎关注每日经济新闻APP
