每日经济新闻 2021-09-17 14:56:22
◎近年来,CD47一直被业内认为是继PD-1/PD-L1之后,肿瘤免疫领域的下一个重要靶点。
◎《掘金创新药》研究员认为,根据临床进度推算,舒格利单抗很有可能成为首家上市的国产PD-L1,基石药业或将抢先崭露头角。但是整体竞争格局不会有明显变化,跨国药企的先发优势仍难以打破,且随着后续适应症拓展,PD-L1本身也会向PD-1市场看齐。
每经记者|金喆 实习生 黄颖琳 每经编辑|魏官红

《掘金创新药》由每日经济新闻联合丁香园Insight数据库共同推出,旨在解读新药研发进展与趋势,剖析产品竞争力与市场前景,洞察医药资本脉络,见证医药产业高质量发展。
根据丁香园Insight数据库统计,9月6日到9月10日,国家药品监督管理局药品审评中心(CDE)共收到5家上市公司提交的5个生物制品新药申请。其中,信达生物递交的CD47-SIRPα单抗IBI397临床申请获受理。

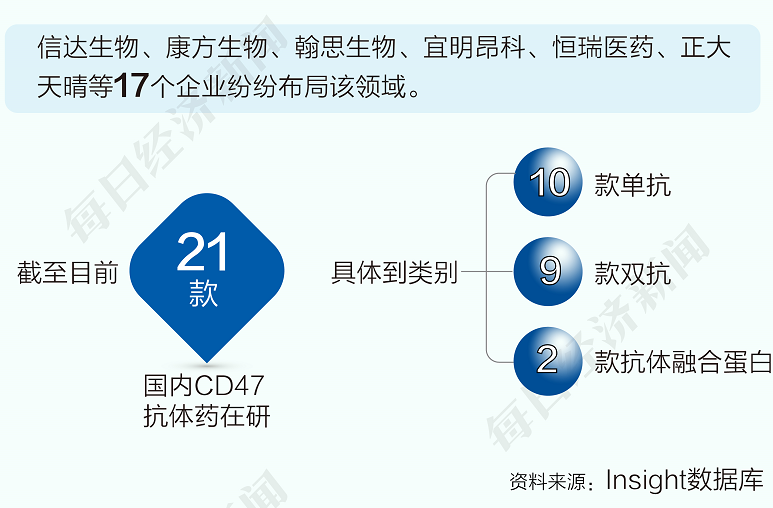
继PD-1/PD-L1之后,Claudin18.2、CD47、CD19等靶点越来越受到重视,竞争环境也日趋激烈。就信达生物申报的IBI397来说,竞争不容小觑,目前共有21款CD47药物进入临床或临床申请,均对获批入场券“蠢蠢欲动”。虽然CD47前景可期,但市场认为入局者太多,或难以形成先发优势,较难复制OK药的市场规模。
此外,虽然资本市场已逐渐对PD-1的利好“脱敏”,而且PD-1与PD-L1可看作同一赛道,但基石药业PD-L1舒格利单抗新适应症上市申请获受理,这一消息还是燃起了投资者的热情,推动药企股价大涨超10%。如能够在今年底顺利面世,基石药业将与其他跨国药企引发新一轮的PD-L1赛道追逐,可超越先发者或成难题。

本周,双鹭药业(002038,SZ)、信达生物(01801.HK)和再鼎医药-SB(09688.HK)各递交1个新药临床申请;以岭药业(002603,SZ)和基石药业-B(02616,HK)等多个药企有新品获批上市。

按申请类别划分,本阶段申报类别情况如下:
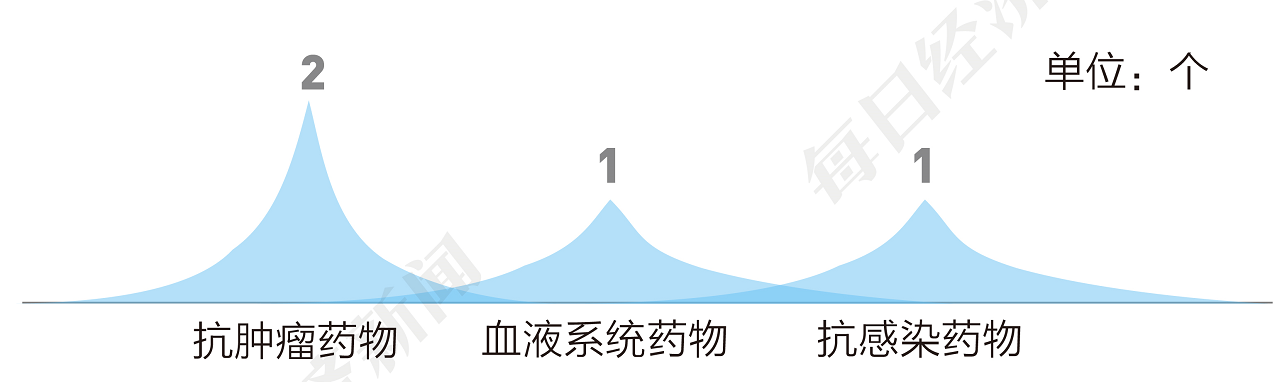
1、信达生物申报国内首款SIRPα单抗,CD47最接近PD-1市场规模
9月8日,信达生物提交的新型抗SIRP-alpha抗体IBI397的临床申请获CDE受理。这是信达生物在2020年3月与临床阶段生物技术公司Alector达成合作引进的产品(Alector研发代号:AL008),根据协议条款,信达生物将主导AL008在中国的开发和商业化,Alector将主导AL008在国外的开发。
IBI397是一种非竞争性抑制SIRP-α/CD47信号的抗体,不会直接阻断信号通路,而是CD47通过与抑制性受体信号调节蛋白α(SIRPα)作用,发出“别吃我”信号,抑制巨噬细胞的吞噬作用,从而保护健康细胞不被免疫系统破坏。
近年来,CD47一直被业内认为是继PD-1/PD-L1之后,肿瘤免疫领域的下一个重要靶点。目前全球范围内尚无CD47药品获批上市,在国内,CD47靶向赛道入局者众多。Insight数据库显示,信达生物、康方生物、翰思生物等17个企业纷纷布局该领域。截至目前,共有21款国内CD47抗体药在研。
信达生物在CD47靶点上又有哪些优势?
信达生物在速度和广度上均占优势,包括CD47单抗IBI-188,具备同类最优(Best-in-class)潜力,适应症为急性髓系白血病(AML)和骨髓增生异常综合症(MDS),当前进度为三期临床;CD47/PD-L1IBI-322,属新型同类首创(First-in-class),适应症为血液肿瘤、晚期/转移性肿瘤,已启动一期临床。如今又增加申报CD47-SIRPα单抗,不难看出信达生物希望“多条腿走路”,做到广泛覆盖。
《掘金创新药》研究员认为,凭借相似的广谱抗肿瘤疗效,CD47药物一旦成功获批上市,其潜在市场规模或将比肩PD-1。至于未来的方向在何处,是单抗、双抗亦或是融合蛋白、联合用药,仍然存有不确定性。
对于未来CD47靶向是否会复制PD-1的竞争局面,深圳森瑞投资管理有限公司研究总监何山则表示,目前普遍认为CD47是下一个最接近PD-1市场规模的品种,但面临的主要问题是这个靶点玩家太多,不像百时美施贵宝的O药和默沙东的K药,有较强的先发优势,所以看单品种可能难有K药这种体量。
从资本市场来看,近期信达生物行情平淡。
图片来源:Wind截图
2、基石药业PD-L1新药上市申请获受理,被纳入港股通后获增持
9月2日,基石药业发布公告称,国家药品监督管理局已受理舒格利单抗用于同步或序贯放化疗后未发生疾病进展的不可切除的III期非小细胞肺癌(NSCLC)患者巩固治疗的新药上市申请(NDA),此次新药上市申请是基石药业递交的第8项新药上市/扩展适应症申请。
与此同时,舒格利单抗治疗IV期NSCLC的NDA已于去年11月获受理,目前正在审评中,预期将于今年年底获批。这意味着,舒格利单抗有望成为全球首个同时覆盖局部晚期/不可切除(III期)和转移性(IV期)非小细胞肺癌全人群的PD-L1单抗。
受此消息影响,9月2日,基石药业股价重回14港元/股以上,涨幅高达10.53%。9月6日,基石药业被纳入港股通名单。截至9月14日,新增港股通持仓146.55万股。
除了肺癌领域,目前舒格利单抗已进行多项注册性临床试验,包括一项针对淋巴瘤的II期注册临床试验,以及四项分别在III期、IV期非小细胞肺癌、胃癌和食管癌的III期注册临床试验。此外,舒格利单抗联合fisogatinib(非索替尼)用于不同适应症的试验也在顺利推进。
关于其市场规模,基石药业海外合作伙伴EQRx公司COO在项目路演时曾提到,舒格利单抗获批后,仅在非小细胞肺癌方面短期内年销售额就可达到20亿美元,如果考虑到后续的其他适应症,如胃癌、食道癌,市场容量在300亿美元。
但是,PD-L1的市场竞争不容小觑。

华创证券研报还提到,到2022年,国内市场有望获批15款PD-1/L1单抗,预计再经过2至3轮医保谈判后,PD-1/L1单抗的年化费用可能下探至2万元至3万元的区间。随着PD-1/L1单抗普药化,PD-1/L1双抗或将成为国内下一阶段免疫治疗的焦点。
封面图片来源:每经记者 王昊毅 摄
如需转载请与《每日经济新闻》报社联系。
未经《每日经济新闻》报社授权,严禁转载或镜像,违者必究。
读者热线:4008890008
特别提醒:如果我们使用了您的图片,请作者与本站联系索取稿酬。如您不希望作品出现在本站,可联系我们要求撤下您的作品。
欢迎关注每日经济新闻APP
