每日经济新闻 2021-11-23 09:21:49
每经记者|陈星 每经编辑|张海妮

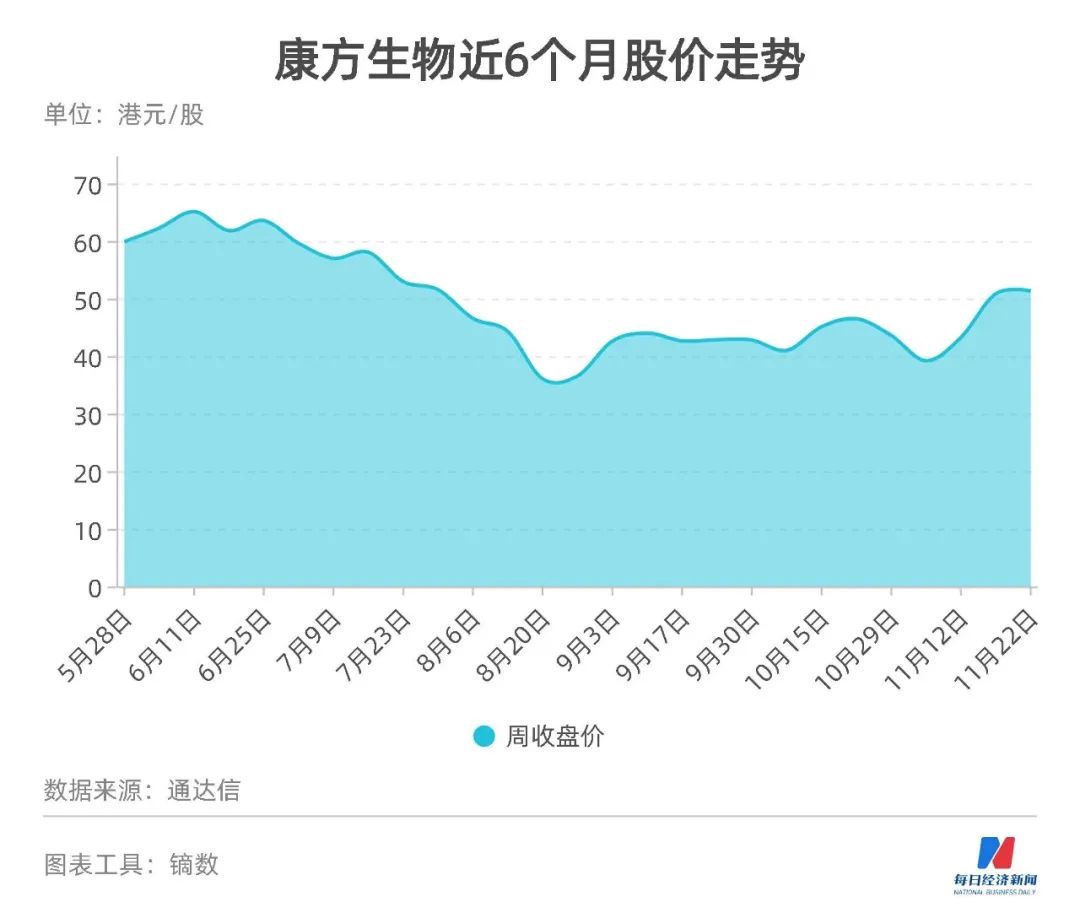
■ 相关公司:康方生物(09926,HK)
■ 核心竞争力:端对端平台(ACE平台);AK104(PD-1/CTLA-4双抗);AK112(PD-1/VEGF双抗)
■ 机构眼中的公司:上半年公司多款产品研发进展顺利,业绩符合预期。公司执行力持续强化,产品陆续进入兑现期
■ 所属概念:生物创新药企业
2010年创建康方生物的夏瑜博士见证了中国创新药工业从起步到提速的全过程。彼时,中国生物制药正在经历从无到有的阶段,一批药企开始研发“me-too”(模仿创新药)类药物,还有少部分以研发“me-better”(跟进创新药)为主的企业,这是创新药研发的初级阶段。
而自2015年药品审评审批制度改革以来,创新药迈入红利期,国内医药企业在药物研发领域成果显著。然而,初始阶段的部分尝试也换来了一些经验与教训。药物同质化竞争、原始创新缺失、创新药商业化前景尚存不确定因素等问题备受关注。
在接受《每日经济新闻》记者专访时,夏瑜表示,国内新药研发的风气起来后,做研发的力量多了,却缺少一个整合的力量,就形成了很多重复投资。这些重复投资不仅占用了大量资金,也占用了大量临床资源。“在同一个适应症上不断用临床资源去做类似的事情,这肯定是资源的浪费。做药的本质本就应当是以临床为导向。”她表示。
随着全球首创的PD-1/CTLA-4双特异性抗体在中国提交上市申请,一开始选择完全自主创新“HARD MODE”的康方生物,将最新的目标定为了从Biotech(生物技术)转型到Big Pharma(大型制药企业)。作为一家创新药企业的掌舵人,夏瑜面临的挑战也从来自实验室变成了来自四面八方。

康方药业。图片来源:公司供图

Big Pharma之路

始于2015年的中国药品审评审批制度改革,至今仍然是中国药物创新领域人士每次聚会时津津乐道的共同话题。正是这场改革,宣告了中国生物制药从无到有,中国创新药正式迈入红利期。
实际上,自药品审评审批制度改革以来,国内医药企业在药物研发领域成果显著。然而,初始阶段的部分尝试也换来了一些经验与教训。药物同质化竞争、原始创新缺失、创新药商业化前景尚存不确定因素等问题也备受关注。
在那场改革之前,2012年,夏瑜和3位友人一同创立了康方生物。这一时期也被誉为中国生物医药新元年,同期诞生的企业,还包括百济神州、信达生物、君实生物等多家本土新一代创新型生物医药企业。
“那时候的研发大多还集中在实验室里,远远没有今天这么热闹。”夏瑜回忆说。
这些初代的创新药企业,通过各种方式希望快速实现企业发展,在药物选择上包括“me-too”、“me-better”,在模式上一部分传统企业或者新生的公司采取“Fast-Follow”甚至license-in模式,快速获得融资,不断把产品推向临床。这些模式,或通过降低药物的开发难度,或压缩开发周期,有利于新药公司迅速构建在研管线,以期实现产品的快速商业化。
与大多数同行不一样的是,康方生物从一开始就选择了困难模式——走完全自主创新的发展道路,从药物发现到工艺开发,再到临床开发和生产销售,这种模式风险相对较大、时间及资金成本高,对于企业的研发实力、抗风险能力都是巨大的考验。
夏瑜曾在公开场合多次强调,“康方至今所有在研管线都是自主研发的新分子候选药物”。为什么是新药,且必须是完全自主研发的新药?
夏瑜表示,国内新药研发的氛围起来后,做研发的力量多了,却缺少一个整合的力量,因此形成了很多重复投资。这些重复投资不仅占用了大量资金,也占用了大量临床资源。“在同一个适应症上不断用临床资源去做类似的事情,这肯定是资源的浪费。做药的本质本就应当是以临床为导向。”她表示。
“以全球市场为目标,以临床价值为导向”开发新药是夏瑜一直秉持的理念。这与夏瑜此前的求学及工作经历相关。在创办康方生物之前,夏瑜在欧美等全球创新前沿阵地积累了21年。夏瑜说,2015年之前,国外先进药物起码要5~10年才能进入中国,而康方生物创办的初衷,本就是希望为以中国患者为首的广大患者带来真正具有创新价值的治疗药物。
如今回首,只做“first-in-class”(首创新药)的思路也显得颇有先见之明。这是因为在创新药蓬勃发展的初始阶段,大量科学家由海外归国,带回了最接近成功或最有前景的研发方向。但相似的选择,却在一定程度上造成了十年后的同质化研发。
中康CMH数据显示,2020年新增临床在研药物最多的前20家企业中,仅有1家没有肿瘤类别的申报,肿瘤总计数量占到了所有适应症的60%。
“这是因为大家都想摘下眼前的好摘的‘果子’,造成大家摘下来的东西都是一样的,可被满足的临床要求被重复满足了,未被满足的临床需求仍未被满足。”有业内人士如是说。这样一来,只有完全“first-in-class”的新药在从实验室迈向市场的过程中,才能更从容,也给企业带来更高的回报率。
坚持自主研发新药的康方正迎来等待已久的收获期。先是今年8月,PD-1药物派安普利单抗获国家药监局批准上市,其联合安罗替尼治疗肺癌一线、肝癌一线还有望成为国内首批大适应症无化疗组合方案;9月,凯得宁单抗用于宫颈癌适应症的上市申请获优先审评。目前,公司共有超过40个临床试验在推进。
有了首个双特异性抗体药物的加持,康方生物在国内的Biotech企业中应该位列第一梯队。但夏瑜的设想还不止于此。在采访中,她透露了康方生物的远景是成为一家中国的“Big Pharma”。在她看来,PD-1是当前肿瘤领域的基石品种,而双特异性抗体是康方生物的护城河,20+在研梯队则是康方生物的殷实底蕴。“我们在肿瘤药以外,还有很多非肿瘤药物在开发中,随着非肿瘤药物健康保障的提高,这些药物未来可能成为康方的主力军”。
而成为一家“Big Pharma”,另一个重要的衡量标准是这家制药企业是否有输出的能力。目前,康方生物的在研管线中,有约10款在开展国际临床。“不管是从国外开始做临床,还是我们尝试寻找License-out以外的方式将药卖到国外,都是在为长远的国际化布局打基础”。

康方生物管线分布(肿瘤学)概况
图片来源:公司官网截图
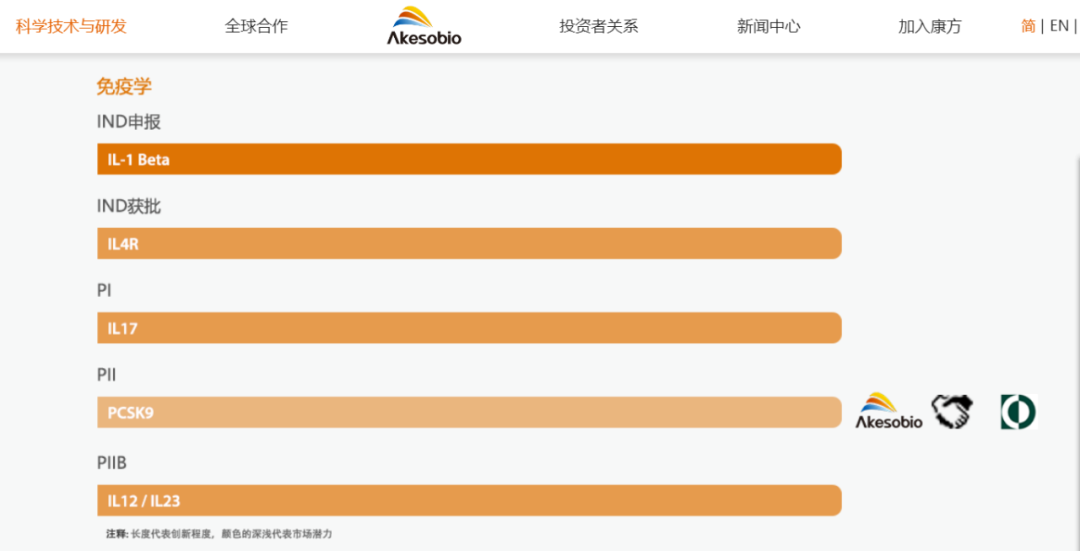
康方生物管线分布(免疫学)概况
图片来源:公司官网截图

中国制药工业正在走向成熟和集约化

自2015年药品审评审批制度改革以来,创新药进入红利期。越来越多的创新药研发企业如雨后春笋般冒出,越来越多的资本将真金白银扑通一声砸了进去。
对科学的追求和看好是好事,但包括夏瑜在内的很多做药人在呼吁着冷静、呐喊着理性,希望这把火能烧得小一点但久一点。
正如中国医药创新促进会执行会长宋瑞霖所言,过去五年,我国创新药量质齐升,但me-too药物同质化竞争、原始创新缺失、创新药商业化前景尚存不确定因素等问题也备受关注。
今年7月,国家药监局药品审评中心(CDE)发布《以临床价值为导向的抗肿瘤药物临床研发指导原则(征求意见稿)》(以下简称《征求意见稿》),强调抗肿瘤药物研发要以临床价值为导向,许多创新药企的股价应声下跌,反映出市场对于新药监管收紧的敏感。
11月19日,CDE官网发布了《以临床价值为导向的抗肿瘤药物临床研发指导原则》(以下简称《指导原则》)。《指导原则》中明确说明“新药研发应以为患者提供更优、更有效、更安全或更便利的治疗选择作为更高目标”。
在采访中,夏瑜说,《征求意见稿》是非常正向的引导,同时也是在一定行业背景下应运而生的。
而除了科学家和企业家以外,资本市场的理性也格外重要。“因为科学家对自己做的事情总是充满了自豪感和热情,这是可以理解的。但资本一定要回归理性,要起到降温和纠偏的作用。以PD-1研发为例,如果资本理性了,在很多地方都可以卡住重复的同类研发。很多早期的PD-1已经把能做的适应症给覆盖了,后面再进入临床的PD-1是很难做的”。夏瑜表示。
而经过新药研发的起步阶段后,国内创新药的形势也发生了一些变化。一些过去几十年靠仿制药赚钱的大药企,开始了本土“买买买”模式。恒瑞医药、正大天晴、石药集团等纷纷与国内创新药企业携手,以真金白银换取后者新药的商业权益。
在集采和资本市场的压力下,寻找新增长点的老大哥们,和长期以科学为导向的创新药企站在了同一个交汇路口。
当记者聊到这一现象时,夏瑜表示,这条路是中国制药工业的必经之路,也是走向成熟化、集约化的体现。在国外制药工业工作多年的夏瑜说,国外有很多的“Biotech”,却很少有企业可以最终成长为“Big Pharma”。原因就是在这个过程中不断有收购、有新的模式产生,这种事情随时都在发生,资本市场也极其认同这样的模式。
“中国制药工业复制这样的模式,对于社会资源而言也是一件正面的事情。有一些创新药企业可能会最终成长起来,有一些就在这个过程中被收购掉了。而目前,国内大药企和创新药企业的合作大多还停留在商业合作层面。在这个层面,大家做的不是相互改变,而是相互借势,将对方的优势发挥到最大化。”她认为。
在康方生物首个药物派安普利单抗上市时,夏瑜就选择与老牌药企正大天晴合作,将这款药物推向市场。

康方生物研发人员 图片来源:公司供图

全球首创PD-1/CTLA-4双特异性抗体药物申请上市

做领头者的坚持迎来了回报。就在采访的前一天,康方生物迎来了一个期待已久的好消息:国家药品监督管理局正式受理全球首创的PD-1/CTLA-4双特异性抗体凯得宁单抗(Candonilimab,研发代号:AK104)用于治疗复发或转移性宫颈癌的上市申请,并获得优先审评。
这意味着,由康方生物自主研发并产业化的凯得宁单抗成为全球首个递交上市申请的基于PD-1的双特异性抗体药物,也成为中国自主研发的首款双特异性抗体药物。
临床研究数据显示,凯得宁单抗治疗经含铂化疗失败的复发或转移性宫颈癌患者的疗效显著,且安全性良好。在目标适应症人群中,凯得宁单抗与已上市的PD-1单抗公开数据相比,显示出更优的疗效。夏瑜在采访中透露,凯得宁单抗有望于明年年中正式获批上市。
在双抗药物领域,凯得宁单抗提交上市申请并获得优先审评具有标志性意义。过去十年间,随着免疫疗法成为肿瘤治疗的主流,以PD-1/L1单抗为代表的免疫检查点抑制剂有更多露出,但尽管PD-1/L1单抗目前已成为十余种肿瘤的标准疗法,但在获批的实体瘤适应症中的有效率普遍在15%~30%,存在有效率不足的问题,这就为以双抗为重要方向的免疫联合疗法提供了登场机会。
尽管潜在机遇广阔,但双抗药物从研发到真正成药存在着巨大的技术壁垒。截至目前,AK104是全球首个进入临床试验的PD-1/CTLA-4双特异抗体。
目前,凯得宁单抗布局的主要适应症还包括胃癌、肺癌、肝癌、食管鳞癌及鼻咽癌等。其中,凯得宁单抗治疗一线胃癌的III期临床也已经正式启动。
“我们当初的指导思想,就是做PD-1做不了的事。”在采访中,夏瑜回忆了凯得宁单抗从立项到递交上市申请的全过程,“在医药工业界,双抗药物开发已经有几十年的历史,但一直存在着较大的技术难关,尤其是进入临床后成药性面临着较大的考验。我们自己有单抗药物的基础,团队也有抗体工程技术的一些经验,因此从2014年前后,康方就开始涉足双抗领域”。
但正如夏瑜所说,实验室里的药物研发是一回事,而能否走到临床阶段并成功获批上市则充满不确定性。药物能否满足未被满足的临床需要也是其最终能否上市的重要衡量指标。
夏瑜说,“凯得宁单抗宫颈癌适应症的病人,首先对准的是二线和三线治疗后失败的宫颈癌病人,这部分群体可以说是真正的未被满足的临床需求”。
作为首创性PD-1/CTLA-4双特异性肿瘤免疫治疗药物,凯得宁单抗旨在实现与肿瘤浸润淋巴细胞(TIL),而不是正常外周组织淋巴细胞的优先结合。在夏瑜看来,凯得宁单抗不仅解决了其基础单抗药物的毒性问题,也使得在治疗性上的可及性更好,“所以不仅仅是1+1>2,而是单个分子的功效已经大于2了”。
从立项到临床、再到申请上市,康方生物是幸运的,因为在实现未被满足的临床需求的过程中,每一个节点都蕴含着可能折戟的危机和需要淌过险滩的勇气与运气。在成药论英雄的创新药行业,康方率先实现了双抗领域的突破。夏瑜坦言,“在实验室里,我们用分子生物学和蛋白质工程的办法组合成另一个蛋白质分子组合,但这离成为一个药还很远。到最后成药,是整个体系在发挥作用,而不是单一环节的功劳。从研发到成药,运气也很重要”。
如今,凯得宁单抗可以说已经进入上市前的冲刺阶段。而面对以研发见长的创新药企业,在新药即将上市时,商业化能力是一个绕不过去的命题。如何让这个全球首创的药物在商业化阶段将其价值最大化,是眼下夏瑜需要考虑的问题。
早前,康方生物的PD-1药物选择与正大天晴合作,借助对方的销售能力推进PD-1的商业化。面对凯得宁,康方生物选择“自己干”。
据夏瑜透露,从去年下半年开始,康方生物开始组建自己的商业化团队,截至目前,这一团队已经超过500人,到今年年底预计将达到近800人。夏瑜称,凯得宁与PD-1的不同之处在于,康方生物甩掉了竞争对手很长时间,在较长一段时期内拥有先发优势。而等到凯得宁真正上市时,自己的商业化团队也趋于成熟。因此,在这个时间点建立自己的销售团队,夏瑜认为是“对的时间”。
卖药当然不仅是招兵买马这样简单。在采访中,能看出来夏瑜将商业销售的问题摆在了与研发同等重要的位置上。按照她的设想,“中国以前没有国产的双抗药物,在宫颈癌免疫治疗的用药经验方面也比较空白,这也是为什么我们要这么早就开始搭建商业化团队,我们从今年开始陆续对一些妇科肿瘤的专科医生做教育普及和学术推广,我们希望借鉴外企的销售模式加上内资企业的销售精神来打造我们的商业化团队”。
而对于重要性不输国内的国际市场,夏瑜说,在考虑License-out的同时,自己同样在基于公司的长远利益和国际化目标考虑,不排除有一些其他路径将凯得宁单抗的利益最大化。正如夏瑜所言,获得优先审评只是凯得宁单抗上市的第一步,眼下,如何加固凯得宁单抗的“护城河”也是她正在思索的问题。

康方生物实验室 图片来源:公司供图

记者手记|做药的本质本就应当是以临床为导向
夏瑜接受采访时,正值康方生物全球首创的PD-1/CTLA-4双特异性抗体在中国提交的上市申请获得优先审评。对于创新药研发企业而言,能够在未被满足的临床需求方面拔得头筹,是实力,也是运气。
“十亿投入,十年研发。”这样的“双十定律”如今依然在上演。而出于对研发风险的规避,一部分模仿型创新、改善型创新也在进行中。采访中,夏瑜说,康方生物之所以选择完全自主创新的“HARD MODE”,就在于她始终认为,在同一个适应症上不断用临床资源去做类似的事情,这肯定是资源的浪费。“做药的本质本就应当是以临床为导向。”她表示。一句以临床为导向,本应是做药的初衷。而随着政策的引导、资本的理性,这个最基本的导向也在做药人的心中更加清晰。
记者:陈星
编辑:张海妮
视觉:蔡沛君
排版: 张海妮 马原
如需转载请与《每日经济新闻》报社联系。
未经《每日经济新闻》报社授权,严禁转载或镜像,违者必究。
读者热线:4008890008
特别提醒:如果我们使用了您的图片,请作者与本站联系索取稿酬。如您不希望作品出现在本站,可联系我们要求撤下您的作品。
欢迎关注每日经济新闻APP
