每日经济新闻 2021-11-22 19:13:46
◎《掘金创新药》研究员认为,双抗药物是未来治疗肿瘤的重要手段,市场潜力巨大,目前国内的双抗行业尚处于从研发向商业化转型的时期;康方生物的双抗管线布局丰富,双抗注射液AK112未来几年有望获批上市,公司有望成为双抗领域的龙头企业。
◎作为国内首个获批治疗外周T细胞淋巴瘤的药物,西达本胺或将再次续约进入医保目录,未来随着更多适应症获批,西达本胺或将进一步实现放量销售。
◎西达本胺是全球首个亚型选择性组蛋白去乙酰化酶(HDAC)抑制剂,可单独或联合其他药物治疗,目前已有两个适应症获批上市,即用于治疗外周T细胞淋巴瘤和乳腺癌,该药品也是微芯生物目前主要的商业化产品和收入来源。
每经记者 金喆 每经实习记者 陈浩 每经编辑 魏官红

《掘金创新药》由每日经济新闻联合药渡数据共同推出,旨在解读新药研发进展与趋势,剖析产品竞争力与市场前景,洞察医药资本脉络,见证医药产业高质量发展。
根据药渡数据,11月8日至14日,国家药品监督管理局药品审评中心(CDE)共收到10家上市公司提交的11个化学新药、治疗用生物制品新药申请。

11月10日,微芯生物发布公告称,西达本胺联合替雷利珠单抗治疗非小细胞肺癌临床申请获受理。2017年进入医保目录后迅速放量的西达本胺也出现在了今年的续约谈判目录之中,适应症为外周T细胞淋巴瘤。作为国内首个获批治疗外周T细胞淋巴瘤的药物,西达本胺或将再次续约进入医保目录。
11月11日,CDE官网显示,康方生物靶向PD-1/VEGFR的双抗药物AK112注射液临床申请获得受理。康方生物曾在11月2日发布公告称,AK112获批开展单药或联合化疗新辅助/辅助治疗可切除非小细胞肺癌的II期临床研究。尽管目前尚未实现盈利,但多家机构表示看好康方生物的商业化前景。资本市场方面或也较为看好AK112的商业化前景,11月2日至今(截至11月22日收盘),公司股价上涨逾三成。

本周上市公司方面,康方生物(09926,HK)共申报2个临床申请,复宏汉霖(02696,HK)、贝达药业(300558,SZ)、翰森制药(03692,HK)、科伦药业(002422,SZ)、海思科(002653,SZ)、微芯生物(688321,SH)、康诺亚(02162,HK)、九典制药(300705,SZ)、复旦张江(688505,SH)各申报1个临床申请。

1.康方生物双抗注射液临床申请再获受理,能否加快公司商业化进程?
11月11日,CDE官网显示,康方生物靶向PD-1/VEGFR的双抗药物AK112注射液临床申请获得受理。此前,康方生物在11月2日发布公告称,公司自主研发的新型肿瘤免疫治疗药物PD-1/VEGF双抗(AK112)获得CDE批准,将开展单药或联合化疗新辅助/辅助治疗可切除非小细胞肺癌的II期临床研究。
据悉,AK112是全球首个进入临床研究阶段的PD-1/VEGF双抗。根据公告,AK112可阻断PD-1与PD-L1和PD-L2的结合,并同时阻断VEGF与VEGF受体的结合,PD-1抗体与VEGF阻断剂的联合疗法已在肾细胞癌、非小细胞肺癌和肝细胞癌等多种瘤种中显示出强大的疗效。鉴于VEGF和PD-1在肿瘤微环境中的共表达,与联合疗法相比,AK112作为单一药物同时阻断这两个靶点,可能会更有效地阻断这两个通路,从而增强抗肿瘤活性。
AK112正在积极拓展多个肿瘤适应症。今年5月,康方生物发布公告称,AK112在中国、澳大利亚等国家开展了剂量爬坡和扩展的I期临床研究后,将再分别开展5项单药或联合用药的临床研究,包括单药治疗晚期非小细胞肺癌、单药治疗复发/转移性妇科肿瘤、联合化疗治疗晚期非小细胞肺癌等。今年10月,AK112获批开展治疗晚期三阴性乳腺癌的临床研究。
继PD-1/PD-L1、CD47、Claudin18.2等热门靶点涌入众多入局者后,双特异性抗体成为当前医药研发的又一大热门赛道。国联证券研报指出,目前全球已经有3个双抗产品正在销售,其中不乏超20亿美元以上的大品种;国内目前已经有35个以上双抗产品进入临床阶段,商业化转化在即,预计国内2030年双抗行业规模超百亿美元。
康方生物是国内双抗领域的领跑者,除AK112,靶向PD-1/CTLA-4的AK104是公司另一款双抗产品,目前AK104的宫颈癌适应症已经提交新药上市申请,并被给予了优先审评资格,有望2022年在国内获批上市。此外,公司还有AK131(PD1/CD73)、AK130(TIGIT/TGFbeta)、AK129(PD1/LAG3)等在研的双抗产品。
目前,康方生物正处于商业化的起步阶段,今年上半年,公司实现收入约1.29亿元,来源于公司CTLA-4单抗对外授权取得的里程碑付款,期内亏损约4.46亿元。此外,公司的派安普利单抗(PD-1)cHL适应症国内已经获批上市,有望快速商业化放量。
尽管目前公司尚未实现盈利,但多家机构表示看好康方生物的商业化前景。兴业证券在研报中表示,康方生物在国内双抗领域处于领先地位,部分产品临床数据优异,亦做到了国际领先;随着AK104的成功,公司将打通双抗的整个研发过程,双抗平台也有望持续产出新的双抗药物;随着各方面能力的建成,公司的发展将进入快车道。
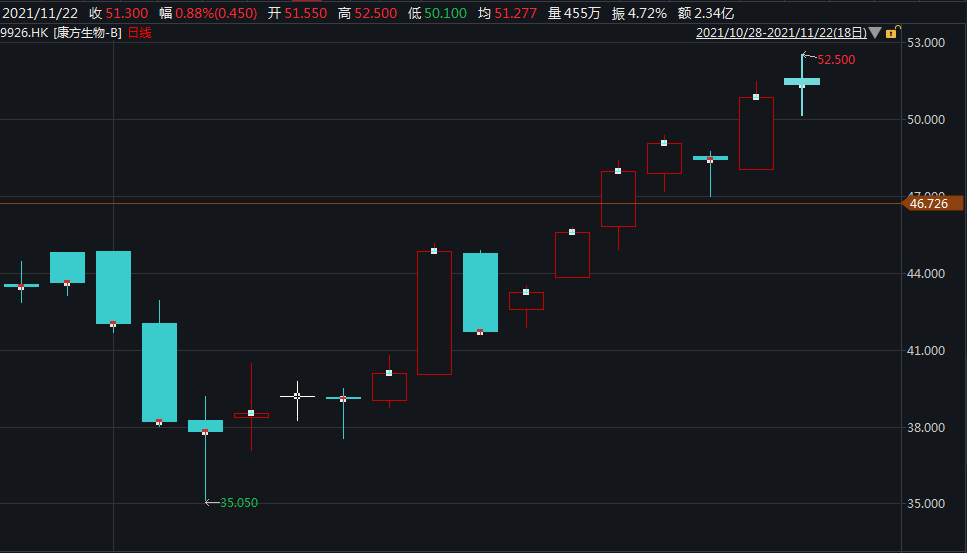
康方生物近期股价走势图 图片来源:Wind截图
《掘金创新药》研究员认为,双抗药物是未来治疗肿瘤的重要手段,市场潜力巨大,目前国内的双抗行业尚处于从研发向商业化转型的时期;康方生物的双抗管线布局丰富,多个双抗产品处于临床或临床前阶段,双抗注射液AK112未来几年有望获批上市,公司有望成为双抗领域的龙头企业。此外,资本市场也较为看好AK112的商业化前景,11月2日至今(截至11月22日收盘),公司股价上涨逾三成。
2.西达本胺联合替雷利珠单抗治疗非小细胞肺癌临床申请获受理,医保续约谈判前景如何?
11月10日,微芯生物发布公告称,公司的西达本胺联合PD-1抑制剂替雷利珠单抗一线治疗PD-L1表达阳性的局部晚期或转移性非小细胞肺癌患者II期临床试验获得受理。
西达本胺是全球首个亚型选择性组蛋白去乙酰化酶(HDAC)抑制剂,可单独或联合其他药物治疗,目前已有两个适应症获批上市,即用于治疗外周T细胞淋巴瘤和乳腺癌。该药品也是微芯生物目前主要的商业化产品和收入来源,2020年实现销售收入2.45亿元,对公司营收贡献超90%。
据悉,西达本胺是国内首个获批治疗外周T细胞淋巴瘤的药物,乳腺癌适应症的获批使西达本胺的适应范围由血液肿瘤拓展到了实体瘤。此次联合百济神州的替雷利珠单抗治疗非小细胞肺癌II期临床试验申请获得受理,加上西达本胺在弥漫大B细胞淋巴瘤III期临床试验的持续推进,西达本胺的适应症范围不断扩大。
11月11日,历时3天的2021年国家医保谈判落下帷幕,此前进入医保后迅速放量的西达本胺也出现在了今年的续约谈判目录之中,适应症为外周T细胞淋巴瘤。微芯生物在投资者互动平台表示,公司今年10月刚刚获批上市的另一款重要产品、以2型糖尿病为适应症的西格列他钠今年不能参加医保谈判。
自2017年进入国家医保目录以来,西达本胺得以快速放量,截至今年上半年,西达本胺累计销售近10亿元。目前,医保谈判结果仍未公布,东吴证券研报指出,无论大分子或小分子药物,今年的整体医保谈判结果好于之前的市场预期,谈判价格鼓励了创新药企业研发和商业化差异化品种的积极性,聚焦差异化创新、抢占先发优势是取得较高定价的关键。
《掘金创新药》研究员认为,作为国内首个获批治疗外周T细胞淋巴瘤的药物,西达本胺或将再次续约进入医保目录,未来随着更多适应症获批,西达本胺或将进一步实现放量销售。
封面图片来源:摄图网-500553887
如需转载请与《每日经济新闻》报社联系。
未经《每日经济新闻》报社授权,严禁转载或镜像,违者必究。
读者热线:4008890008
特别提醒:如果我们使用了您的图片,请作者与本站联系索取稿酬。如您不希望作品出现在本站,可联系我们要求撤下您的作品。
欢迎关注每日经济新闻APP
